Ablation pharmaco-mécanique (MOCA) vs ablation thermique de la grande veine saphène : 1ère étude randomisée contrôlée monocentrique.
Alors que l’ablation thermique termine tout juste son implantation en France avec la publication des nouvelles cotations pour le laser endoveineux (LEV), se pose déjà la problématique du traitement de référence des varices après celui-ci. Plusieurs dispositifs relevant de stratégies différentes sont à la lutte : la colle au cyano-acrylate, la phlébogriffe,… et dans le cas de cet article : l’ablation pharmacomécanique (APC), en anglais MOCA (mecanochemical ablation).
METHODE
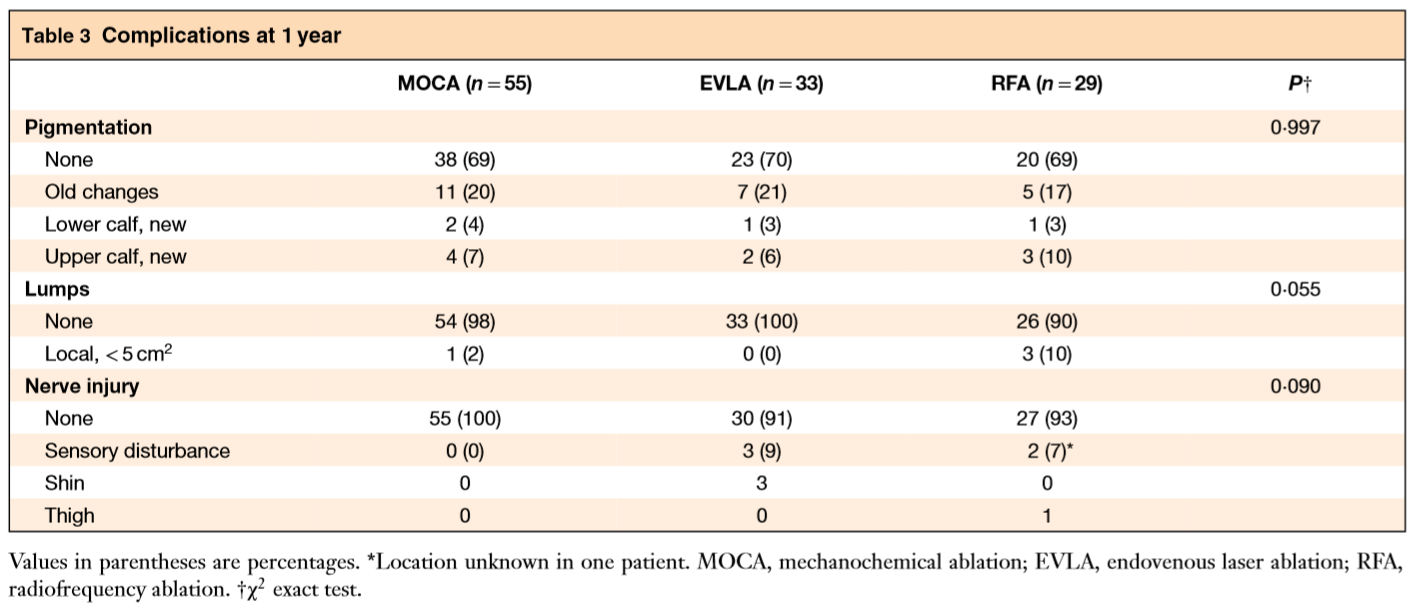
C’est le dispositif ClariVein® de Merit Medical®, encore non commercialisé en France, que cette équipe finlandaise d’Helsinki a choisi d’évaluer dans cette étude. Il permet d’agresser la paroi de la veine variqueuse à la fois mécaniquement par l’agitation de l’extrémité d’un guide et chimiquement en injectant un sclérosant liquide (photo 1), du sodium tetradecyl sulfate (STS) à 1.5%. Cette étude compare l’APC à l’ablation thermique par laser endoveineux Biolitec® (70 J/cm) et radiofréquence (RF) VNUS Closure Fast® (2 cycles sur le 1er segment puis 1 cycle par segment) dans le traitement de la grande veine saphène dans le cadre d’un protocole d’essai randomisé monocentrique avec suivi à 1 an. Les traitements se déroulaient sous médication par Fentanyl, Diazépam et Propofol. Les tributaires étaient traitées par phlébectomies concomitantes sous tumescence dans les 3 groupes. Les critères d’inclusion et d’exclusion étaient classiques pour ce type d’étude. La randomisation avait lieu par enveloppes scellées. Il n’y avait pas d’aveugle.
RESULTATS
Les groupes de patients étaient comparables en termes de classification CEAP, obésité, diamètre de la GVS à mi-cuisse et impact des varices sur la qualité de vie (clinical disability score). Le taux d’occlusion à 1 an, critère principal de l’étude, était de 100% pour le LEV, 100% pour la RF et 82% pour l’APC. Il y avait donc 10 cas de recanalisation au moins partielle dont 7 qui concernaient le segment proximal. Les auteurs ont identifié un diamètre significativement plus élevé pour ces 7 patients à 8.6 mm en moyenne versus 6.5 mm en moyenne pour les occlusions complètes à 1 an du même groupe.
Les médications utilisées pour l’APC l’étaient dans les mêmes proportions que le thermique pour Fentanyl et le Diazépam (tableau 1). Le Propofol n’a été utilisé que pour les patients traités par RF. La quantité de tumescence était nettement inférieure pour l’APC car utilisée juste pour la phlébectomie. Il n’y avait pas de différence significative sur la quantité d’antalgiques pris en post-procédure.
Il n’y a aucune complication thrombo-embolique veineuse dans aucun groupe. Les auteurs rapportent 1 cas d’infection superficielle, sans préciser s’il s’agissait d’un érysipèle ou d’une autre infection, jugulée par antibiothérapie orale. Les pigmentations résiduelles après APC étaient de l’ordre de 20%, un taux équivalent aux groupes thermiques. Il n’y a logiquement eu aucun trouble neurologique avec l’APC, contrairement au thermique qui rapportait un taux de 9% pour le LEV et de 7% pour la RF (tableau 2).
DISCUSSION
Les auteurs ne manquent pas de remarquer que leur taux d’occlusion avec l’APC à 82% est nettement inférieur à ce qui est relevé dans les séries publiées dans la littérature (88 à 95%) ce qui s’avère effectivement décevant. Mais cela a été confirmé dans un 2nd essai randomisé publié 1 mois après cet article : l’équipe néerlandaise d’Holewijn (1) a trouvé un taux d’occlusion de 84% à 1 an et 80% à 2 ans.
L’explication des auteurs finlandais repose à la fois sur l’échec des troncs les plus gros et sur un caractère opérateur-dépendant du traitement qui serait supérieur à celui du thermique, mieux standardisé. L’équipe néerlandaise explique, elle, un défaut d’efficacité, également sur le segment proximal, par l’utilisation de polidocanol à la place du STS, non disponible dans leur pays.
Les conclusions finlandaises qualifient de moins douloureux le traitement par APC sur le fait que le propofol n’a pas été utilisé pour ces patients, oubliant qu’il n’a pas été non plus utilisé pour les patients traités par LEV. Bref, le schéma de leur étude ne leur permet pas réellement d’arriver à cette conclusion. Bien sûr, l’absence d’aveugle pour les patients mais surtout pour l’évaluation du résultat dans le suivi est un biais notable de cet essai. Nous regrettons par contre l’absence de taux d’occlusion à 3 ans pour une étude publiée en 2019 et dont les inclusions se sont terminées en 2015, car le maintien dans le temps du résultat à 1 an est également un point important pour l’efficacité du traitement.
Qu’apporte cette étude ?
Tout d’abord que le thermique a encore de beaux jours devant lui car il est difficile de faire aussi bien que les très bons scores d’occlusions à 5 ans dont il bénéficie. Ce 1er essai randomisé montre un taux de succès inférieur à celui annoncé par les séries précédentes pour l’APC. Toute nouvelle thérapeutique sur la thématique ne peut espérer que faire au moins aussi bien que le thermique et l’on voit déjà le débat dans la littérature se profiler sur les à-côtés : moins de complications (déjà faibles), meilleur confort du patient et temps plus court de traitement par l’absence de tumescence, la non-utilisation d’un bloc opératoire. Sur ces points, cette étude montre que les nouvelles techniques restent lestées par la stratégie thérapeutique des tributaires, encore souvent basée dans la littérature sur les phlébectomies concomitantes. Or ce traitement complémentaire semble gommer le bénéfice d’un nouveau traitement du tronc (taux de fentanyl, diazépam et tumescence identique pour l’APC que pour le LEV pour la douleur dans cette étude). En somme : quel intérêt pour le patient d’avoir un traitement indolore du tronc si c’est le traitement de la tributaire dans le même temps qui lui fait mal ? Le traitement qui concerna aussi bien le tronc que les tributaires aura donc les meilleurs chances de s’imposer face au thermique. A moins que l’on ne se recentre autour d’autre stratégie thérapeutique : traitement différé ou non-traitement des tributaires. Le débat sur ces stratégies continue.
Dans le cas du ClariVein®, le procédé se heurte également aux limites de l’utilisation d’un produit sclérosant, ici le STS, certes sous forme liquide, mais liquide agitée par la partie mécanique. Il n’est donc pas sûr que cette thérapeutique s’affranchisse complètement des complications de type phosphènes, migraines ou accident vasculaire cérébral connues pour la sclérose à la mousse. Or l’incidence de ces complications est tellement faible qu’elle passe sous le seuil de détection de ces études à effectifs limités. Aussi seule l’utilisation massive en vraie vie pourra nous rassurer sur ce point.
De nouvelles données sont à attendre de 2 essais randomisés en cours et qui devraient être publiés en 2020, l’un comparant le ClariVein® à la colle au cyanoacrylate et l’autre le comparant au LEV.
Référence
Holewijn S, van Eekeren RRJP, Vahl A, de Vries JPPM, Reijnen MMPJ; MARADONA study group. Two-year results of a multicenter randomized controlled trial comparing Mechanochemical endovenous Ablation to RADiOfrequeNcy Ablation in the treatment of primary
great saphenous vein incompetence (MARADONA trial). J Vasc Surg Venous Lymphat Disord. 2019 May;7(3):364-374.
Photo 1 : Représentation commerciale de l’extrémité du guide du ClariVein® dans la varice par Merit Medical®.
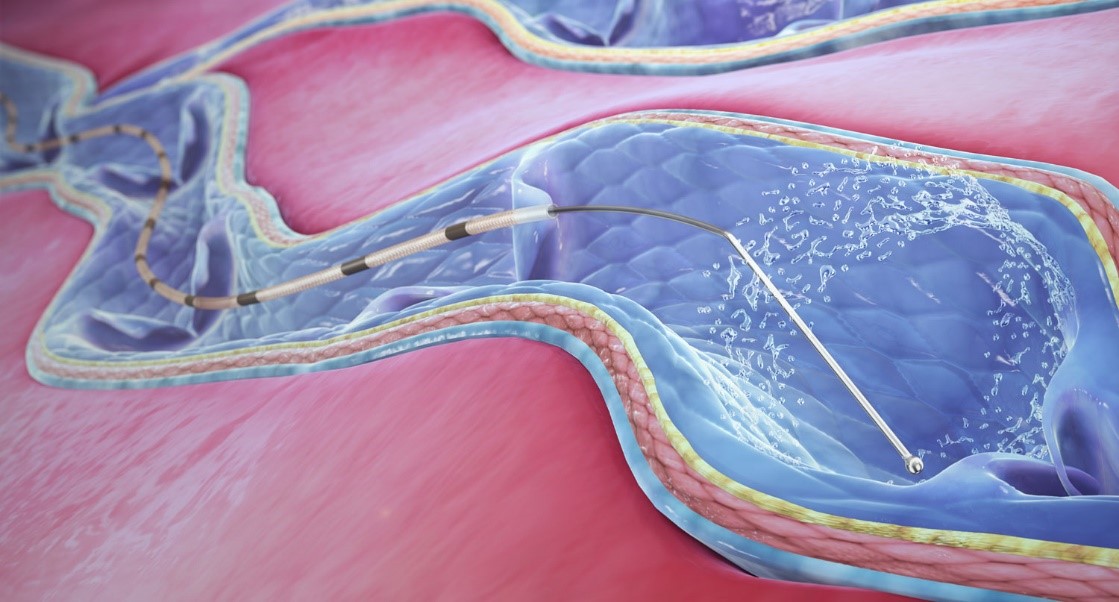
Tableau 1 : Traitements médicamenteux utilisés durant la procédure
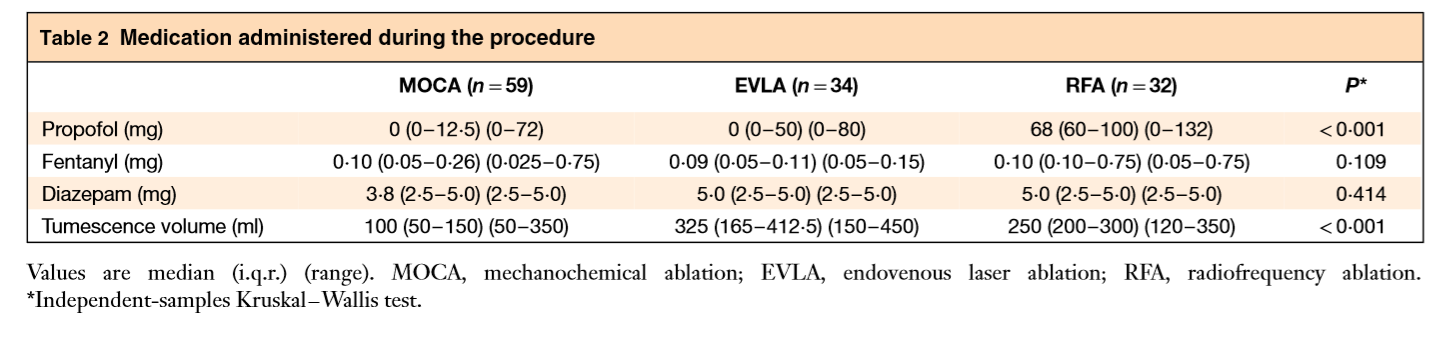
Tableau : Complications à 1 an