Elaboration d'un score du halo dans la maladie de Horton : évaluation de l'efficacité diagnostique et corrélation avec l'ischémie oculaire.
L’artérite giganto-cellulaire (AGC) (maladie de Horton) est une maladie auto-immune caractérisée par l’inflammation des vaisseaux de gros calibre. L’ischémie oculaire en est la principale complication. Les examens biologiques révèlent une inflammation systémique avec une CRP élevée, une anémie et une thrombocytose.
La Ligue européenne contre le rhumatisme (EULAR) recommande une exploration par ultrasons des artères temporales et axillaires en première intention pour les patients suspect d’artérite giganto-cellulaire. Le signe du halo est le critère diagnostic principal, caractérisé par un épaississement hypoéchogène, homogène de la paroi artérielle. Sa sensibilité et sa spécificité par rapport au diagnostic clinique sont de 77 et 96%. On sait peu de choses sur la relation entre l’extension des localisations artérielles visualisées en écho-Doppler et la sévérité de la maladie. On retrouve dans la littérature une relation entre l’extension des localisations et l’intensité de la perte de poids, mais pas de corrélation entre l’atteinte temporale et le risque de complications oculaires. Dans une autre étude, l’atteinte axillaire semble associée avec un faible taux de complications oculaires. L’objectif de cette étude était d’évaluer la corrélation entre l’extension des localisations et la sévérité de la maladie, en comptant le nombre de sites présentant un halo au niveau des artères temporales et des artères axillaires, afin de développer un score du halo intégrant le nombre de halos et l’épaisseur maximale de la paroi en fonction de chaque siège anatomique. Ces critères sont confrontés à l’intensité de l’inflammation et la survenue d’accidents oculaires.
METHODE
C’est une étude monocentrique prospective conduite au sein du département de rhumatologie du Southend University Hospital de juin 2010 à décembre 2013. Cent quatre patients suspects d’être atteints d’une artérite giganto-cellulaire ont bénéficié d’une exploration par écho-Doppler et d’une biopsie de l’artère temporale au plus tard dans les 7 jours qui ont suivi la mise en route d’une corticothérapie. Ils ont bénéficié d’une réévaluation à 6 mois.
L’évaluation écho-Doppler est réalisée par un seul examinateur confirmé qui ne connait pas l’état clinique du patient. Un panel d’experts évalue la qualité de l’iconographie en relecture. Le signe du halo est défini par un aspect hypoéchogène circonférentiel autour de la lumière vasculaire. Un score du halo est développé sur la base du percentile de l’épaisseur de la paroi maximale au niveau du halo le plus gros en fonction du site.
RESULTATS
Sur les 104 patients vus à l’admission, 92 ont bénéficié de l’exploration écho-Doppler et de la biopsie de l’artère temporale et 89 ont été réévalués à 6 mois. Parmi ces 89 patients, le diagnostic d’artérite giganto-cellulaire a été établi chez 58 d’entre eux (Tableau 1).
Les trois segments des deux artères temporales ainsi que les deux artères axillaires ont été explorés par écho-Doppler. Un signe du halo a été mis en évidence sur 41 segments d’artère temporale commune, 29 segments pariétaux, 32 segments frontaux et 14 artères axillaires. L’épaisseur maximale du halo était mesurée. Le score du Halo est développé à partir des 20èmes, 40èmes, 60èmes et 80èmes percentiles de l’épaisseur maximale mesurée pour chaque segment (Tableau 2). Le score global est calculé en faisant la somme des gradations pour chaque territoire, avec un coefficient 3 pour l’atteinte axillaire. Le score du halo varie de 0 à 48 (Figure 1).
Le nombre de halos et les scores du halo sont de manière significative supérieurs chez les patients qui ont présenté une atteinte confirmée par rapport aux sujets indemnes. Le nombre de halos et le score du Halo ont une efficacité diagnostique similaire par rapport au diagnostic clinique (aire sous la courbe > 0.70). On retrouve une spécificité de 95% par rapport à l’estimation clinique en considérant un nombre de halo ≥ 6 et un score ≥10. Si un score ≥ 10 a été retrouvé chez 12 patients (21%), seulement 2 patients (3%) présentaient un nombre de halos ≥ 6. Le rapport de vraisemblance positif pour un score ≥ 10 est élevé (LR+ 0.641) mais faible (1.07) pour un nombre de halo ≥ 6 (Figure2).
Le nombre et l’épaisseur des halos sont supérieurs chez les patients présentant une biopsie de l’artère temporale positive. Les deux critères présentent une bonne fiabilité dans la prédiction d’un résultat positif à la biopsie (aire sous la courbe > 0.80). On retrouve la même pertinence si on ne considère que les halos au niveau des artères temporales.
Il n’y a pas été mise en évidence de différence pour les patients présentant une artérite giganto-cellulaire traitée par corticoïdes, que l’examen soit fait à J0-J1, J2-J3 ou J4-J7.
On ne retrouve pas de corrélation entre le nombre de halos avec le taux d’hémoglobine, mais une corrélation positive avec le taux de CRP et de plaquettes. Le score du halo est encore mieux corrélé avec le taux de CRP, a une corrélation positive avec le taux de plaquettes et négative avec le taux d’hémoglobine. Ces résultats sont moins probants si on ne considère que les artères temporales. L’atteinte des artères axillaires semble donc être associée plus grandement avec un syndrome inflammatoire général (Figure 3).
On retrouve une corrélation indépendante entre l’ischémie oculaire (atteinte neurologique antérieure ou postérieure), le sexe masculin et le nombre de halos et le score. Un nombre de halos ≥ 2 et un score ≥ 3 présentent une excellente sensibilité, mais une faible spécificité pour prédire une ischémie oculaire, avec un rapport de vraisemblance positif < 2. On retient qu’un faible nombre de halos et un faible score permettent de définir les patients à faible risque. Cette évaluation est identique lorsqu’on ne considère que les artères temporales, ce qui confirme l’indépendance entre l’atteinte axillaire et les accidents oculaires. En considérant indépendamment le nombre de halos et le score en prédiction d’accidents oculaires, un nombre de halos ≥ 2 présente un OR d’ischémie oculaire de 12 (95% CI= 1,430 à 100,705 ; P= 0,022), un score ≥ 3 présente un OR d’ischémie oculaire de 9,88 (95% CI= 1,137 à 85,887; P= 0,038).
DISCUSSION
L’exploration des artères temporales et des artères axillaires permettent une estimation raisonnable de l’extension de la maladie. Le score permet de poser un diagnostic d’artérite giganto-cellulaire plus fortement que le simple comptage. L’atteinte axillaire est corrélée à une inflammation générale. Les formes diffuses sont à plus haut risque d’accident oculaire (> 30%) ; les patients avec un faible nombre de halos et un faible score présentent un faible risque d’accident oculaire (≤ 5%), ce qui représente la moitié des patients de l’étude.
L’extension de la maladie est directement corrélée à l’inflammation systémique, il y a une corrélation forte entre le score du halo et le niveau de CRP et de plaquettes, meilleure qu’avec le nombre de lésions.
L’évaluation du score montre une sensibilité de 78% et une spécificité de 55-61% pour le diagnostic d’artérite giganto-cellulaire. Si on considère un score ≥ 10, on obtient une spécificité voisine de 95%, ce qui pourrait envisager d’utiliser cette technique en remplacement de la biopsie.
On retrouve dans l’étude une prévalence de comptes et de scores élevés chez les hommes probablement du fait que la paroi des artères est plus épaisse chez les hommes que chez les femmes. Dans cette étude, ont été retenus les halos dont l’épaisseur était inférieure à 1mm au niveau des artères axillaires.
Il n’y a pas été retrouvé de différence chez les patients ayant bénéficié d’une corticothérapie durant une semaine par rapport aux patients non encore traités. Ceci se conçoit du fait que le halo disparait après quelques semaines à quelques mois de traitement. On n’observe que peu de disparition de halo au niveau des artères axillaires.
Enfin, les examens étaient réalisés par un opérateur expérimenté ne connaissant pas l’état de la maladie, la reproductibilité intra et inter-observateur n’a pas été évaluée et devrait faire l’objet d’un prochain travail.
COMMENTAIRES
Dans cet article, les auteurs ont pour objectif d’établir un score reproductible permettant un diagnostic de certitude écho-Doppler de l’existence d’une artérite giganto-cellulaire, d’apprécier son extension et d’en calculer le risque oculaire qui est la complication la plus sévère. Les auteurs comparent les critères écho-Doppler aux critères diagnostics de l’European League Against Rheumatism (EULAR) (1,2). Ces recommandations proposent la réalisation de l’écho-Doppler en première ligne des actes d’imagerie en cas de suspicion clinique. Les signes retenus sont la présence d’un signe du halo avec une artère incompressible (Tableau 3). Dans ces recommandations, il est spécifié que l’écho-Doppler doit concerner l’étude des artères temporales et des artères axillaires. Les critères retenus sont inspirés de l’OMERACT (Outcome Measures in Rheumatology working group) qui définit le halo comme une image homogène hypoéchogène bien délimitée de la paroi artérielle, circonférentielle autour de la lumière vasculaire, visualisée sur une coupe transverse et sur une coupe longitudinale. Cette description présente une sensibilité de 77% et une spécificité de 96% par rapport à l’estimation clinique. La visualisation d’une sténose ou d’une occlusion de l’artère temporale n’influe pas sur la valeur diagnostique de la présence du halo. L’exploration des artères axillaires est d’une grande aide au diagnostic en cas d’exploration temporale négative ou non contributive chez les sujet fortement suspects.
La technique d’exploration est bien définie par les critères exposés au sein de la Tabul study (3). Cette étude avait pour but d’optimiser les critères diagnostiques de la biopsie de l’artère temporale et de l’écho-Doppler quel que soit l’état du patient par rapport à un traitement par corticoïde, une durée de traitement supérieure à 5 jours diminuant sensiblement la sensibilité de l’écho-Doppler avec présence de plus de faux négatifs. L’objectif premier de l’étude était d’évaluer les performances diagnostiques de l’écho-Doppler et d’en apprécier le caractère d’outil diagnostic alternatif à la biopsie. L’objectif secondaire était l’évaluation économique de cette attitude. Cette étude nécessitait avant inclusion pour l’écho-Doppler une accréditation des centres par évaluation à distance d’acquisitions sur sujets sains, puis sujets atteints selon un protocole prédéfini. Il y avait une évaluation inter-observateur des deux techniques, écho-Doppler et anatomopathologie des biopsies. Les résultats de l’étude étaient appréciés sur une analyse avant la deuxième semaine et à 6 mois après le diagnostic clinique. Les résultats entre l’écho-Doppler et la biopsie étaient discordants chez 115 patients (30%) en faveur de l’écho-Doppler. En rapportant chacune des techniques au diagnostic clinique, on retrouve une sensibilité de 54% (95% CI 48%-60%) et une spécificité de 81% (95% CI 73%-88%) pour l’écho-Doppler versus diagnostic clinique, la sensibilité de la biopsie temporale étant de seulement 39% (95% CI 33%-46%) et sa spécificité de 100% (95 CI 97-100%). Ceci peut s’expliquer par l’atteinte focale des artères touchées, la biopsie ne regardant qu’une partie de l’artère temporale, l’écho-Doppler exhaustif explorant tous l’arbre artériel.
Dans cette étude, l’analyse économique est fonction du coût, de la sensibilité des techniques, des différentes situations cliniques (selon les complications retrouvées : accidents oculaires, AVC, mortalité en rapport avec l’artérite giganto-cellulaire), des traitements utilisés et leur iatrogénie (HTA, diabète, fractures…) (Tableaux 4,5), ainsi que la qualité de vie. La stratégie optimale concernant le coût de la maladie est conditionnée par le jugement clinique… La stratégie incluant clinique et ultrasons est la plus performante, probablement du fait du coût de l’exploration (Tableau 6). Les conclusions de cette étude sont un bénéfice de 456 £ par patient en faveur de l’attitude diagnostique privilégiant l’écho-Doppler soit environ 4,735,000 £ par an pour le Royaume Uni. Il semble donc que l’écho-Doppler ait une place privilégiée dans l’attitude diagnostique des artérites giganto-cellulaires du fait de sa performance, de son innocuité et de son moindre coût.
Qu’en est-il en France ? Le parcours national de soin (PNDS) (4) concernant l’artérite giganto-cellulaire relève une prédominance féminine (3 femmes pour 1 homme), préconise un bilan inflammatoire axé sur la PCR et le fibrinogène, mais pas sur le taux d’hémoglobine et le taux plaquettaire et confirme le fait que les complications ophtalmiques sont le plus à craindre. Les signes à la biopsie restent positifs jusqu’à 4 semaines après la mise en route d’une corticothérapie. Comme dans toutes les recommandations, il est nécessaire que le diagnostic soit réalisé par un opérateur expérimenté, que ce soit l’écho-Doppler ou l’analyse histologique. En cas de signes ophtalmologiques, une corticothérapie à forte dose doit être instaurée (1mg/kg/j vs 0,7mg/kg/j). Les atteintes nerveuses ophtalmiques (neuropathie optique ischémique) sont le plus souvent antérieures (9 fois sur 10), c’est plus rarement une thrombose de l’artère centrale de la rétine. La valeur retenue pour l’élévation de la CRP est de 25 mg/L alors qu’elle est de 50 mg/L dans l’article de van der Geest et la VS discriminante est de 50 mm/h alors qu’elle n’est évoquée dans l’article que pour dire son non-intérêt.
L’artérite giganto-cellulaire est définie comme une artérite segmentaire et focale, ce qui explique les faux négatifs à la biopsie de l’artère temporale lorsque celle-ci est réalisée sans repérage échographique au préalable. Enfin, ce texte revendique pour l’écho-Doppler une sensibilité de 54% et une spécificité de 81%
Il apparaît donc évident que l’écho-Doppler, et on peut presque dire l’échographie vasculaire du fait du seul élément recevable aux vues de la littérature qu’est le signe du halo, est un outil diagnostic performant. Il doit être réalisé par des praticiens expérimentés avec du matériel adapté, sonde de haute voire très haute fréquence. Le signe du halo est fortement en faveur d’une artérite giganto-cellulaire, plus que les sténoses et les thromboses que l’on retrouve aussi en cas de pathologie athéromateuse. L’examen doit concerner les artères temporales, mais aussi la carotide externe, les artères vertébrales et les artères axillaires. Quant au score du halo décrit dans l’article, il reste à valider tant sur le plan interne qu’externe. Des questions restent en suspens, pourquoi retenir comme valeur pour les artères axillaires une épaisseur pariétale ≤ 1 mm ? est-ce significatif ? Pourquoi attribuer un coefficient de 3 pour l’atteinte axillaire ? ce n’est pas expliqué dans l’article. On conçoit que le risque ophtalmique soit supérieur en cas d’atteinte des artères temporales par rapport aux artères axillaires et que l’inflammation générale soit importante chez les patients ayant plusieurs axes atteints par rapport à ceux qui ont uniquement une atteinte des artères temporales localisée aux artères temporales.
Tableau 1 : Caractéristiques des patients.
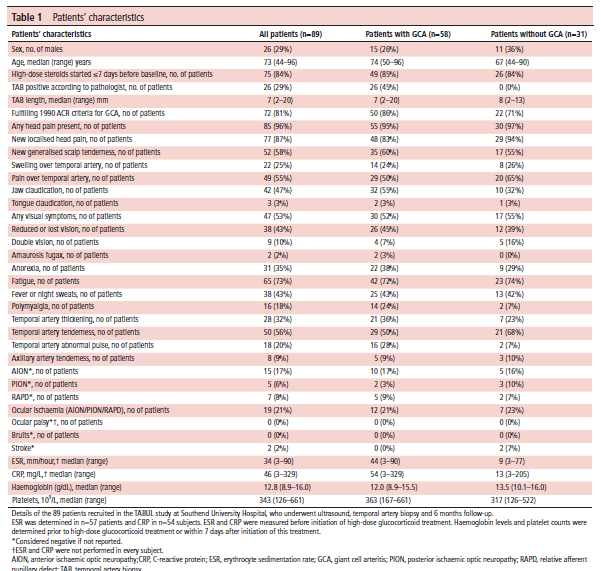
Tableau 2 : Score du Halo : valeurs retenues en fonction du site et de l’épaisseur du halo. Les valeurs s’échelonnent de 0 à 4.
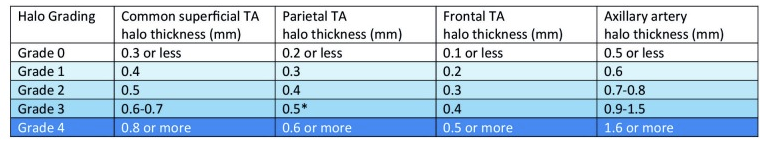
Figure 1 : Score du halo. Chaque score est rapporté sur un schéma. Le score correspond à la somme des scores des différents territoires avec un facteur multiplicatif de 3 pour les atteintes axillaires.
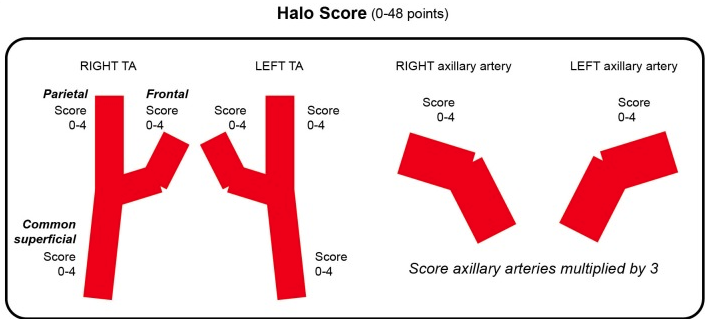
Tableau 3 : Recommandations de l’European League Against Rheumatism (EULAR).
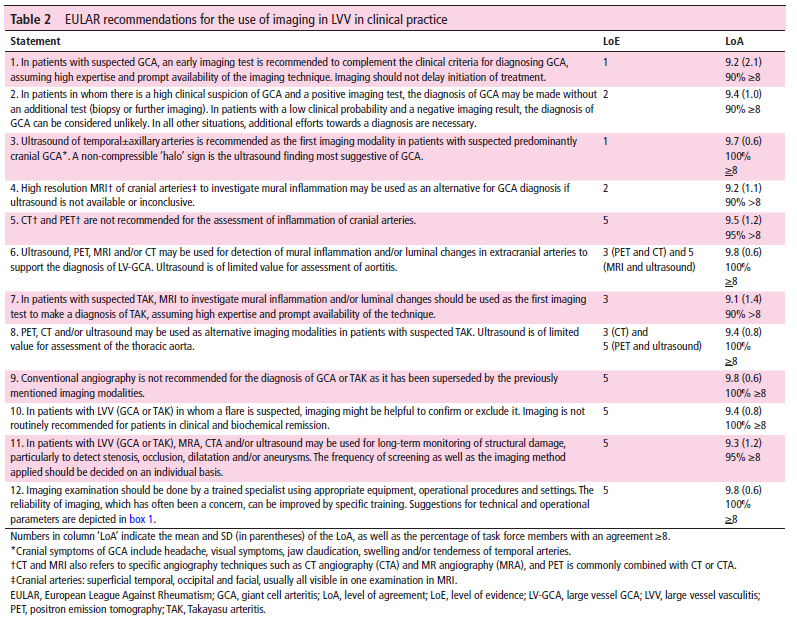
Tableau 4 : Coût annuel (en £) en fonction des complications oculaires (étude TABUL).
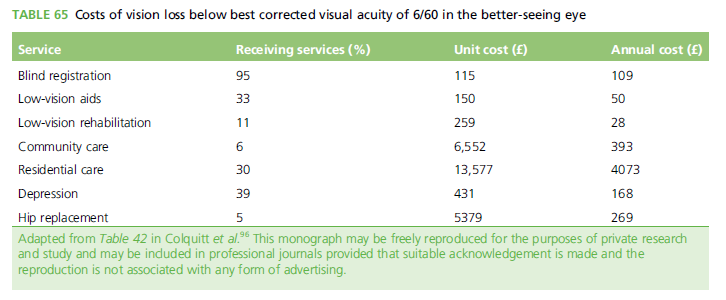
Tableau 5 : Surcoût en rapport avec la iatrogénie d’un traitement par corticothérapie (étude TABUL).
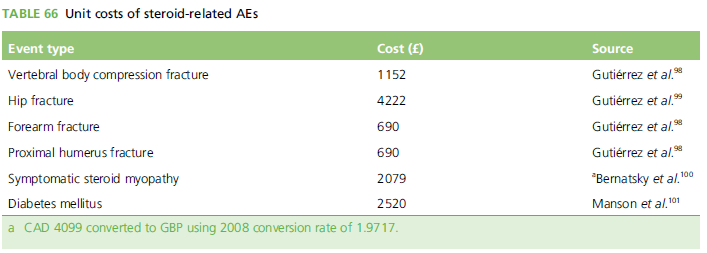
Tableau 6 : Coût et qualité de vie.

Références
- 1. Dejaco C et al ; EULAR recommendations for the use of imaging in large vessel vasculitis in clinical practice. Ann Rheu Dis 2018 ;77 :636-643.
- 2. Bardi M et al ; EULAR recommendations for the use of imaging in large vessel vasculitis in clinical practice summary. La radiologia medica (2019) 124 :965-972.
- 3. Lugmani R et al ; The role of Ultrasound Compared to Biopsy of Temporal Arteries in the Giant Cell Arteritis (TABUL) : a diagnostic accuracy and cost-effectiveness study. Health Technology Assessement vol 20 Issue 90 November 2016.
PNDS artérite à cellules géantes 2017 (Filière de Santé des Maladie Auto-Immunes et Auto-Inflammatoires rares (FAI
